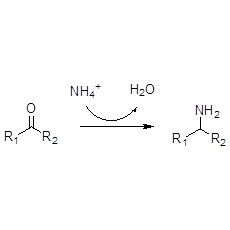
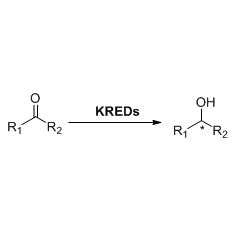
Ene reductază (ERED)
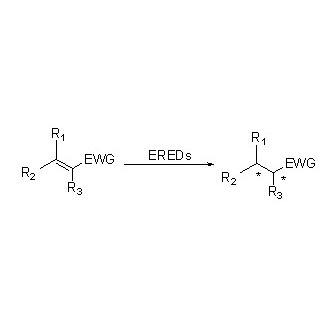
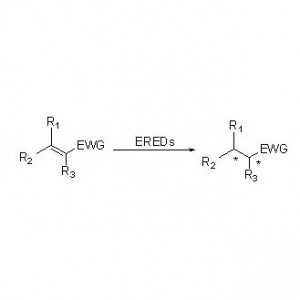
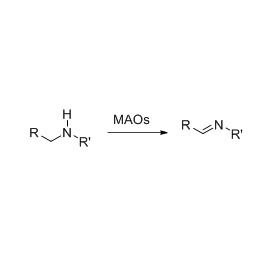
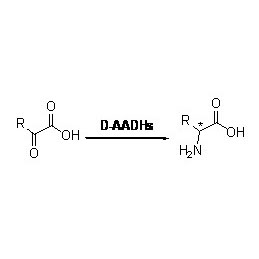
ES-ERED-urile catalizează diverse tipuri de substraturi datorită spectrului larg de substraturi. În general, legăturile duble C=C ale compușilor α, β-nesaturați cu grupări absorbante de electroni (inclusiv aldehidă cetonică, grupări nitro, acizi carboxilici, esteri, anhidride, lactone, imine etc.) sunt ușor reduse de ES-ERED-uri, dar legăturile duble inactivate nu.
Există 46 de tipuri de produse enzimatice ERED (numărate ca ES-ERED-101 ~ ES-ERED-146) dezvoltate de SyncoZymes.
Mecanism catalitic:
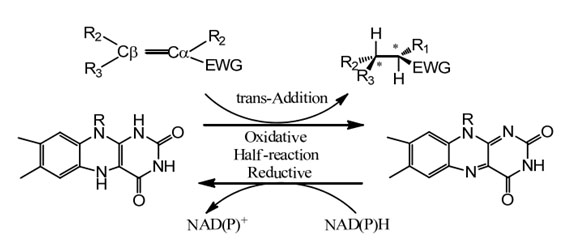
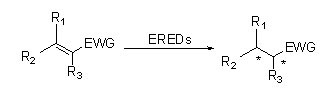
| Enzime | Cod produs | Specificații |
| Pudră enzimatică | ES-ERED-101~ ES-ERED-146 | un set de 46 de Ene Reductaze, câte 50 mg fiecare 46 de articole * 50 mg / articol sau altă cantitate |
| Kit de screening (SynKit) | ES-ERED-4600 | un set de 46 de Ene Reductaze, câte 50 mg fiecare 46 de articole * 50 mg / articol sau altă cantitate |
★ Specificitate ridicată a substratului.
★ Selectivitate chirală puternică.
★ Conversie ridicată.
★ Mai puține produse secundare.
★ Condiții de reacție blânde.
★ Prietenos cu mediul.
★ Siguranță ridicată.
➢ În mod normal, sistemul de reacție ar trebui să includă substrat, soluție tampon (pH optim de reacție), coenzime (NAD(H) sau NADP(H)), sistem de regenerare a coenzimelor (de exemplu, glucoză și glucoză dehidrogenază) și ES-ERED.
➢ Toate ES-ERED-urile pot fi testate respectiv în sistemul de reacție de mai sus sau cu kitul de screening ERED (SynKit ERED).
➢ Toate tipurile de ES-ERED care corespund diferitelor condiții optime de reacție ar trebui studiate individual.
➢ Substratul sau produsul cu concentrație mare poate inhiba activitatea ES-ERED. Cu toate acestea, inhibarea poate fi ameliorată prin adăugarea în loturi de substrat.
Exemplul 1 (aldehide sau cetone α,β-nesaturate)(1):
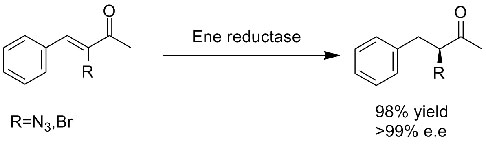
Exemplul 2 (acizi carboxilici α,β-nesaturați și derivații acestora)(2):
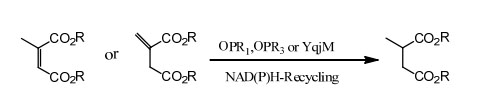
A se păstra 2 ani sub -20℃.
Nu contactați niciodată condiții extreme, cum ar fi: temperatură ridicată, pH ridicat/scăzut și concentrație mare de solvent organic.
1. Lucídio C, Fardelone J, Augusto R, e tal. J.Mol.Catal.B:Enzym., 2004, 29: 41-45.
2. Stueckler C, Hall M, Ehammer H, și alții. Org. Lett, 2007, 9(26): 5409-5411.